علماء يربطون الخلايا الفردية بالإلكترونيات العضوية
نجح باحثون في جامعة لينشوبينغ (Linköping) السويدية في إنشاء اتصال وثيق بين الخلايا الفردية والإلكترونيات العضوية. وتضع هذه الدراسة، التي نُشرت في مجلة Science Advances، الأساس لعلاج الأمراض العصبية وغيرها من الأمراض في المستقبل بدقة عالية جدًا. كما تتيح مراقبة النشاط الخلوي والتحكم فيه بدقة. نستعرض في هذه المقالة النتائج الأساسية لهذه الدراسة، ودراسات أخرى سابقة لها، مع أهم الاختراقات والتطبيقات لهذا المجال الواعد.
التحكم بالدماغ:
يتم التحكم بالدماغ عن طريق الإشارات الكهربائية التي يتم تحويلها إلى مواد كيميائية في التواصل بين خلايا الدماغ. ومن المعروف منذ فترة طويلة أنه يمكن تحفيز أجزاء مختلفة من الدماغ بمساعدة الكهرباء. ولكن غالباً ما تكون الطرق غير دقيقة وتؤثر على أجزاء كبيرة من الدماغ. في بعض الأحيان، تكون هناك حاجة إلى أقطاب كهربائية معدنية لإصابة الجزء الصحيح من الدماغ بدقّة، ما ينطوي على خطر أن يؤدي القطب الكهربائي الصلب إلى إتلاف أنسجة الدماغ أكثر من مجرّد نقل الإشارة، وهذا ما قد يسبب التهاباً أو تندباً.
قراءة مقترحة
يمكن أن يتضمن الحل لعلاج أجزاء معينة من الدماغ مواد بوليميرية عضوية موصلة بهدف الجمع بين الأنظمة الحيوية والأقطاب الكهربائية. ونظراً لأن البوليمرات لينة ومتطابقة حيويًا، ويمكنها نقل كل من الكهرباء والأيونات، فهي أفضل من الأقطاب الكهربائية التقليدية.
التحكم بالدماغ عن طريق إشارة كهربائية
دراسات سابقة:
لقد جرت محاولات سابقة لتثبيت الإلكترونيات العضوية على سطح الخلية، ولكن باستخدام خلايا معدلة وراثيًا تجعل الأغشية أكثر تقبلاً. في دراستهم الحالية، لم يستخدم الباحثون خلايا معدلة وراثيًا ومع ذلك تمكنوا من تحقيق اقتران محكم دون التأثير على وظائف الخلية الأخرى. وهذه هي المرة الأولى التي يتم فيها ذلك. والطريقة هي استخدام عملية من خطوتين حيث يتم أولاً استخدام جزيء التثبيت لإنشاء نقطة ربط في غشاء الخلية. وفي الطرف الآخر من الجزيء يوجد هيكل يمكن أن يلتصق فيه قطب البوليمر نفسه.
وتتمثل الخطوة التالية في البحث في الحصول على نقطة تثبيت موزعة ومستقرة بشكل متساوٍ ومستقر على الغشاء ومعرفة كيف يتصرف اقتران البوليمر مع مرور الوقت.
الاختراقات الرئيسية:
1- الإلكترونيات الحيوية العضوية للواجهات أحادية الخلية:
يستخدم العلماء البوليمرات الموصلة أو الترانزستورات الكهروكيميائية العضوية لإنشاء واجهات ناعمة ومتوافقة حيوياً مع الخلايا.
على عكس الإلكترونيات الصلبة القائمة على السيليكون، فإن المواد العضوية مرنة وتحاكي الأنسجة البيولوجية، ما يقلل من تلف الخلايا.
2- مراقبة النشاط الخلوي في الزمن الحقيقي:
يمكن لهذه الأجهزة الكشف عن الإشارات الكهربائية (على سبيل المثال، إطلاق الخلايا العصبية، وتقلصات الخلايا العضلية) أو التغيرات الكيميائية (على سبيل المثال، إطلاق الناقلات العصبية). فيمكن مثلاً لجهاز استشعار عضوي صغير متصل بخلايا عصبية تسجيل نبضاتها الكهربائية بدقة عالية.
3- التحفيز الدقيق للخلايا المنفردة:
يمكن للإلكترونيات العضوية أيضًا توصيل محفزات كهربائية أو كيميائية للتلاعب بسلوك الخلية.
التطبيقات الأساسية للإلكترونيات الحيوية العضوية أحادية الخلية:
1- علم الأعصاب وواجهات الدماغ والآلة:
- التسجيل والتحفيز أحادي الخلية العصبية: يمكن للترانزستورات العضوية الكشف عن نشاط الخلايا العصبية الفردية وتعديلها، ما يساعد في علاج الاضطرابات العصبية (مثل مرض باركنسون والصرع).
مثال: استخدمت دراسة أسلاكًا نانوية من مادة PEDOT:PSS للتسجيل من الخلايا العصبية بأقل ضرر ممكن.
- دراسات عضويات الدماغ: تراقب الإلكترونيات العضوية كيفية استجابة "الأدمغة المصغرة" المزروعة في المختبر للأدوية.
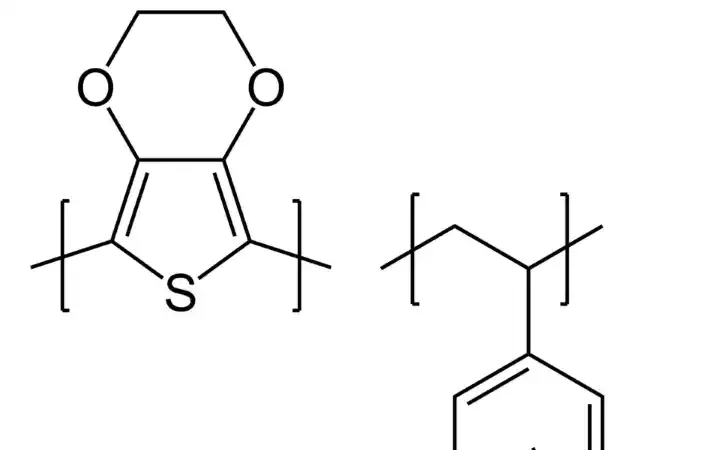
التركيب الكيميائي لبوليمير PEDOT:PSS (Poly(3,4-ethylenedioxythiophen) polystyren-sulfonat)
2- الطب الدقيق واختبار الأدوية:
- فحص العقاقير أحادية الخلية: أجهزة الاستشعار العضوية تتبع كيفية استجابة الخلايا السرطانية أو خلايا القلب الفردية للعلاجات.
مثال: تستخدم رقاقة الهندسة الطبية الحيوية في الطبيعة ترانزستورات كهروكيميائية عضوية لاختبار فعالية العلاج الكيميائي على خلايا الورم المفردة.
- الطب الشخصي: يتم اختبار الخلايا المشتقة من المريض لاختبار تفاعلات الأدوية قبل العلاج.
3- إصلاح القلب والفيزيولوجيا الكهربائية:
- اللصاقات القلبية الذكية: أقطاب كهربائية عضوية تكتشف وتصحح عدم انتظام ضربات القلب على مستوى الخلية الواحدة.
مثال: استخدمت دراسة للمواد المتقدمة شبكة بوليمر موصلة لاستعادة الإيقاع في أنسجة القلب التالفة.
4- الجهاز المناعي وأبحاث السرطان:
- مراقبة هجمات الخلايا المناعية: أجهزة الاستشعار العضوية تتبع كيفية تفاعل الخلايا التائية مع الخلايا السرطانية في الوقت الحقيقي.
- الكشف المبكر عن السرطان: تكتشف المستشعرات الحيوية العضوية فائقة الحساسية المؤشرات الحيوية التي تطلقها الخلايا السرطانية المفردة.
5- علم الأحياء التركيبي والبرمجة الخلوية:
- التحكم الكهربي: تقوم الأجهزة العضوية بتوصيل إشارات كهربائية لتحفيز التعبير الجيني في خلايا منفردة.
مثال: استخدمت دراسة الإلكترونيات الحيوية العضوية لتنشيط كريسبر في خلايا محددة.
نشاط عصبي متوهج، يُظهر مسارات عصبية معقدة واتصالات داخل شبكة معقدة
التحديات والحلول الرئيسية:
1- التوافق الحيوي والاستقرار على المدى الطويل:
يمكن أن تتحلل المواد العضوية (مثل PEDOT:PSS) أو تؤدي إلى استجابات مناعية. ويكمن الحلّ في البوليمرات ذاتية الشفاء، وهي مواد جديدة تصلح الأضرار الطفيفة في الجسم الحي. وكذلك يمكن استعمال الطلاءات مثل بولي إيثيلين أو أكسيد الجرافين لأنها تحسن الاستقرار وتقلل من الرفض المناعي.
2- إمدادات الطاقة وكفاءة الطاقة:
تحتاج الأجهزة الإلكترونية الحيوية الصغيرة إلى مصادر طاقة فعالة وطويلة الأمد. يمكن هنا استعمال البطاريات القابلة للتحلل (على سبيل المثال، البطاريات القائمة على المغنيسيوم) لأنها تذوب بعد الاستخدام. من جهة أخرى، يمكن استعمال الأجهزة التي تعمل بحركات الجسم أو الجلوكوز.
3- قابلية التوسع والتصنيع:
من الصعب تصنيع الإلكترونيات العضوية النانوية لملايين الخلايا. يكمن الحلّ في الطباعة ثلاثية الأبعاد للإلكترونيات العضوية، أو في تصنيع اللفائف لإنتاج الإلكترونيات الحيوية المرنة بكميات كبيرة.
4- تداخل الإشارات والضوضاء:
تضيع الإشارات الخلوية الضعيفة في "الضوضاء" الحيوية. وهنا يمكن استخدام خوارزميات التعلم الآلي التي تعمل على تصفية الضوضاء وتعزيز اكتشاف الإشارات. كما أن الأقطاب الكهربائية النانوية تعمل على تحسين نسبة الإشارة إلى الضوضاء.
5- الاندماج مع الأنسجة الحية:
هذا يعني ضرورة ضمان التواصل السلس بين الإلكترونيات والجسم الحيوي. يتمّ ذلك إمّا عن طريق الواجهات الهجينة الحيوية، وذلك بزراعة الخلايا مباشرة على الدوائر العضوية؛ أو عن طريق التجميع الموجه بالحمض النووي، وهو توجيه الإلكترونيات النانوية للارتباط بخلايا محددة.
الاتجاهات المستقبلية:
- غرسات قابلة للتحلل بالكامل للمراقبة/التحفيز المؤقت.
- أنظمة الدارة المغلقة القائمة على الذكاء الاصطناعي: الأجهزة التي تضبط العلاج تلقائيًا بناءً على بيانات الخلايا في الوقت الفعلي.
- التجارب البشرية للغرسات الإلكترونية الحيوية العضوية (على سبيل المثال، لإصابات الحبل الشوكي).